 北交所IPO审核问答30条全文公开!负面行业清单出炉!
北交所IPO审核问答30条全文公开!负面行业清单出炉!
发布日期:2022-05-16浏览次数:2560
 高粮价预警:用不起化肥,全球水稻产量将减产10%
高粮价预警:用不起化肥,全球水稻产量将减产10%
发布日期:2022-04-21浏览次数:2245
 中小企业经营调查:多地出台“纾困”计划,期待打通物流“堵点”
中小企业经营调查:多地出台“纾困”计划,期待打通物流“堵点”
发布日期:2022-04-21浏览次数:2202
 人民币中间价连续两日下调 不存在长期贬值的基础
人民币中间价连续两日下调 不存在长期贬值的基础
发布日期:2022-04-21浏览次数:2154
发布日期:2022-11-22浏览次数:1168
发布日期:2022-12-06浏览次数:1015
发布日期:2022-05-13浏览次数:968
发布日期:2022-08-25浏览次数:964
发布日期:2022-12-01浏览次数:922
发布日期:2022-05-13浏览次数:921
目录
《Acumen Pharmaceuticals Inc》
目录
一、 基本面分析
1.1 公司简介
1.2 公司团队
二、 生物学背景
2.1 阿尔兹海默症(AD)概述
2.2 淀粉样蛋白
2.3 单克隆抗体
三、 技术平台
3.1 主要技术平台
3.2 平台的主要优势
四、 公司管线
4.1 临床前数据及临床实验进程
4.2 竞争情况
五、 融资与合作情况
六、 财务状况
七、 小结
一、基本面分析
1.1 公司简介
Acumen Pharmaceuticals Inc.是一家处于临床前阶段的生物技术公司,创立于1996年,总部位于美国弗吉尼亚州Charlottesville,侧重于淀粉样蛋白β寡聚体(AβOs)治疗阿尔兹海默症(AD)。
公司的专有技术平台用于开发候选产品,候选产品ACU193能够阻断AβOs毒性,以满足一项重大的医学需求:治疗轻度痴呆症或阿尔茨海默症导致的轻度认知障碍。
公司的唯一在研管线是ACU193,其是靶向Aβ蛋白寡聚体的IgG2m4单抗,是其与 Merck & Co., Inc.(Merck)合作开发的,通过阻止Aβ蛋白寡聚体结合树突棘,减缓神经元功能衰退,指征阿尔兹海默症,计划在2022年年底之前产生有关安全性、耐受性的临床数据。
该公司于2021年7月1日在美国纳斯达克上市,发行价为16美元,发行1000万股,募集资金1.6亿美元,股票代码ABOS。
1.2 公司团队
Daniel O’Connell担任公司总裁兼CEO。O’Connell获得了布朗大学的学士学位和弗吉尼亚大学的工商管理硕士学位。他曾参与创立并担任为阿尔茨海默病开发深部脑刺激疗法的临床阶段公司Functional NeuroModulation Ltd.的CEO。他还是投资于初创的神经科学公司的NeuroVentures Capital, LLC 的创始成员和前任管理合伙人。
Matthew Zuga担任公司CFO和CBO。Zuga获得了北卡罗来纳大学教堂山分校凯南-弗拉格勒商学院的 MBA 学位和俄亥俄州立大学的工商管理/金融学士学位。Zuga于2020年6月至2021年6月间担任HighCape Capital Acquisition Corp的CFO和COO以及 HighCape的董事会成员。他自2013年10月起为HighCape Capital, LLC的合伙人。他于2019 年7月至2021年4月间担任Acumen公司顾问。目前Zuga也是Aziyo Biologics, Inc.董事会成员。
Eric Siemers担任公司首席医疗官(Chief Medical Officer),并从 2018 年 4 月起担任公司的顾问。Siemers以最高荣誉获得印第安纳大学医学院的医学博士学位。他于1998年11月至2017年12月间供职于礼来,负责多项阿尔茨海默病化合物的临床试验,包括五项三期研究以及一期和二期研究。此前,Siemers博士创立了主要研究帕金森病和亨廷顿病的印第安纳大学Movement Disorder Clinic。Siemers博士还曾任职于NIA/阿尔茨海默病协会工作组,该工作组基于生物标志物和临床症状提出了阿尔茨海默病的新研究命名法。他还是阿尔茨海默病协会研究圆桌会议创始成员、阿尔茨海默病神经影像计划指导委员会成员。
Russell Barton任公司的COO。Barton获伊利诺伊州立大学的化学学士学位和普渡大学的化学硕士学位。他还兼任AgeneBio临床运营总监。他于1979年至2017年间供职于礼来,并于2007年至2017年长达10年间担任该公司全球阿尔茨海默病平台团队的COO官。Barton还曾参与旨在促进全球阿尔茨海默病相关企业CEO与纽约科学院之间的合作的全球阿尔茨海默病平台的设计和启动。
Acumen的管理团队拥有深厚的科学和药物开发背景,并致力于为患者开发安全有效的疗法。同时他们还有为上市公司和风险投资支持的临床阶段公司以及大型生物制药公司(如礼来)领导临床开发项目的丰富经验。
二、生物学背景
2.1 阿尔兹海默症(AD)概述
阿尔茨海默症(Alzheimer’s disease,AD)是最常见的神经退行性疾病。临床上以记忆障碍、失语、失用、失认、视空间技能损害、执行功能障碍以及人格和行为改变等全面性痴呆表现为特征,痴呆症的50%-75%是由阿尔茨海默症造成的(痴呆症包含了多种类型,如阿尔茨海默病,血管性痴呆症和帕金森性痴呆症等)。65岁以前发病者,称早老性痴呆;65岁以后发病者称老年性痴呆。阿尔茨海默症目前在美国影响超过 600 万人,现在是美国第六大死因,如果没有更有效的治疗方法,它的排名可能会继续上升。根据国际阿尔茨海默病协会发布的报告显示,2015年全球新发990万阿尔茨海默症患者,总数约为4600万人。预计阿尔茨海默症患者的人数将在2030年和2050年分别增至7500万和1.315亿,全球每年需要为阿尔茨海默症支出的费用达到了8180亿美元。每3秒全世界就会增加1名阿尔茨海默症患者,每100位60岁及以上人口中就有5-8名阿尔茨海默症患者,而截止2017年底,我国60岁以上的老年人口已经达到2.41亿。
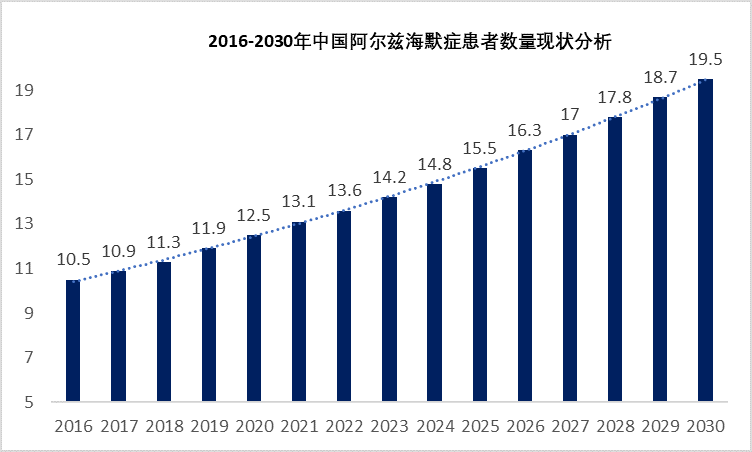
图片来源:Insight数据库
中国阿尔兹海默症患者数量现状分析
美国食品药品管理局(FDA)此前批准的5种抗阿尔茨海默症的主要药物——多奈哌齐(donepezil)、利凡斯的明(rivastigmine)、加兰他敏(galantamine)、他克林(tacrine)、美金刚(memantine),都只能延缓其发展(他克林的副作用较大,所以目前治疗中已不再使用)。这些药物均为2003年(含)之前获批,从2003年至2021年的18年间没有任何一款成功的治疗阿尔兹海默症的药物上市。
2.2 淀粉样蛋白
几十年来的AD研究的主要假设即淀粉样蛋白假说,认为产生AD的原因是Aβ肽单体积累到有助于细胞内神经原纤维形成的细胞外淀粉样蛋白斑块中,引起tau蛋白缠结,进而引起炎症,最终导致神经元细胞死亡并造成进行性痴呆。基于这一假设,许多正在开发的用于AD的单克隆抗体主要针对Aβ单体或淀粉样蛋白斑。
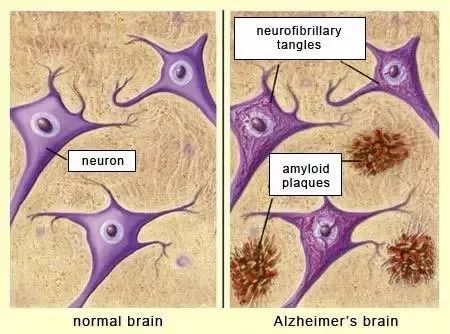
图片来源:McGill大学
正常人与AD患者脑神经对比
在阿尔茨海默病患者中,已经确定了三个主要的淀粉样蛋白 - β(Aβ) 种类库:Aβ单体、Aβ低聚物(AβO)和纤维状Aβ聚集体(斑块)。在过去十年中,Aβ单体以及Aβ斑块一直是阿尔茨海默氏症药物开发工作的主要焦点,而鲜有人关注AβO。

图片来源:公司官网
三种主要的淀粉样蛋白
但最近但研究表明,AβO会破坏大脑回路并阻止神经元正常放电。AβO的积累与突触退化和丢失、tau磷酸化和炎症有关。现在,压倒性的科学证据表明,AβO是毒性最强的淀粉样蛋白,会导致记忆和认知障碍以及慢性神经变性,现在被称为阿尔茨海默病的标志。最近的实验室研究表明,从神经系统中消除AβO可使受损的回路恢复某些功能。
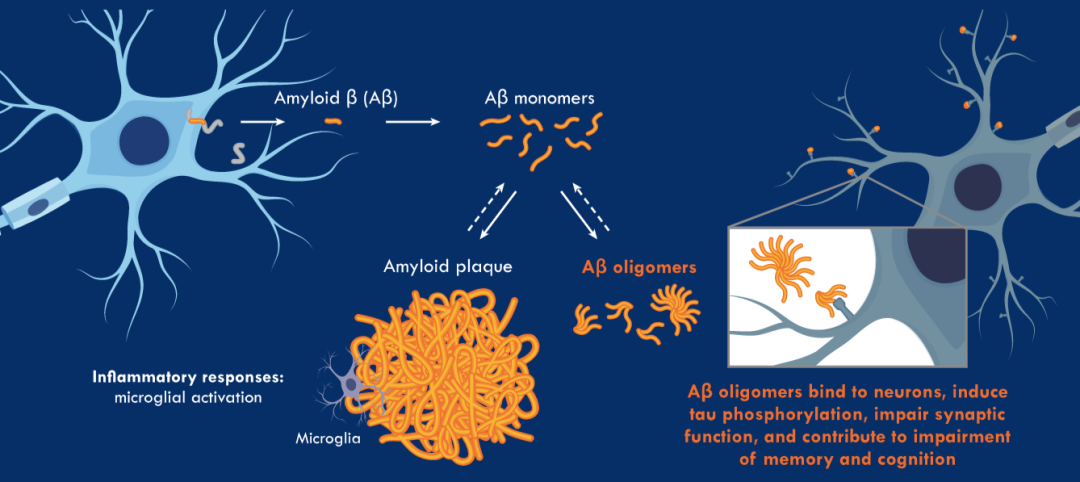
图片来源:公司官网
AβO作用机制
2.3 单克隆抗体
单克隆抗体是由单一B细胞克隆产生的高度均一、仅针对某一特定抗原表位的抗体。通常采用杂交瘤技术来制备,杂交瘤(hybridoma)抗体技术是在细胞融合技术的基础上,将具有分泌特异性抗体能力的致敏B细胞和具有无限繁殖能力的骨髓瘤细胞融合为B细胞杂交瘤。用具备这种特性的单个杂交瘤细胞培养成细胞群,可制备针对一种抗原表位的特异性抗体,即单克隆抗体。单克隆抗体优点有纯度高、灵敏度高、特异性强、交叉反应少、制备的成本低。单克隆抗体的制备可应用于以下用途:(1)凝集实验:haemaglutination;(2)沉淀反应:Precipitation reaction;(3)ELISA 等免疫学检测;(4)亲和层析:分离蛋白质;(5)免疫印记(western blotting);(6)免疫沉淀;(7)BIAcore biosensor:检测Ab-Ag或与蛋白的亲和力;(8)放射免疫学方法检测免疫复合物;(9)磁珠分离细胞;(10)流式细胞仪:用于细胞的分型和细胞分离;(11)临床疾病的诊断和治疗。
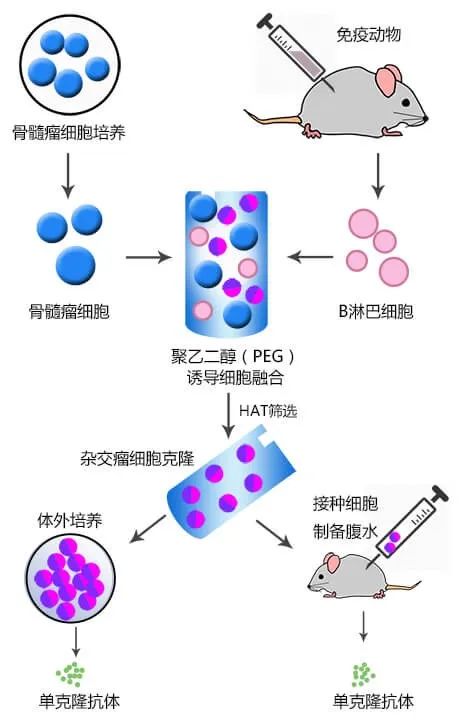
图片来源:德泰生物
单克隆抗体生产流程
三、技术平台
3.1 主要技术平台
公司的主要技术平台为用于在研产品管线ACU193的技术平台。ACU193是一种抗淀粉样蛋白-β寡聚体(AβO)单克隆抗体(mAb),在阿尔茨海默症中具有一流的疗效和安全性。ACU193被工程化修饰以减少免疫效应器功能信号,对Aβ寡聚体有高选择亲和性(是单体的500倍以上,表位由Aβ寡聚体内Aβ单体的N端构型组成),并避免与血管淀粉样蛋白结合以减少ARIA(淀粉样蛋白相关成像,大脑水肿或微出血)。它可能缓解阿尔茨海默症患者的症状。ACU193 通过阻止AβO与树突棘结合并帮助保护神经元功能来解决阿尔茨海默症的潜在原因。ACU193是第一个被发现和开发的针对可溶性AβO的临床阶段人源化单克隆抗体,是与Merck & Co., Inc.为期八年的研究合作的结果。研发团队认为ACU193代表了一种与当前和先前AD免疫疗法不同的方法,因为它对AβO具有高度亲和力。ACU193对AβO具有纳摩尔级别的亲和力,对AβO的亲和力比对Aβ单体高出约500倍,同时对淀粉样蛋白斑亲和力有限,或完全不亲和。

图片来源:蹊之美股生物医药
ACU193作用机制
3.2 平台的主要优势
ACU193是Acumen和Merck为期八年的研究合作的结果,Acumen拥有其专有权。在Acumen团队的管理下,研究人员进一步分析了ACU193的体内活性和可开发性。2017年,美国国家老龄化研究所向Acumen提供了360万美元的U01竞争性赠款,用于ACU193的临床前和早期临床开发。
ACU193与其他抗淀粉样蛋白单克隆抗体相比具有如下优势:
1.相对于其他特异性较低或靶向不同的淀粉样物质(如单体或斑块)的抗淀粉样蛋白单克隆抗体,ACU193对低聚物(有毒的AβO物质)具有高度特异性;
2.ACU193旨在提高临床疗效,降低ARIA(淀粉样蛋白相关成像异常)风险;
3.除可以减缓疾病外,ACU193还具有改善认知的潜力。
四、公司管线
基于上述平台,公司研发了候选产品ACU193管线。
4.1 临床前数据及临床实验进程
在Acumen与Merck合作进行的非临床研究中,ACU193的表现很好,展现出了其作为AD治疗方法的潜力。ACU193具有高亲和力,研究表明,相比于Aβ单体,它对AβO的亲和力超过500 倍。一项对AD患者的脑组织进行的离体研究显示,ACU193与淀粉样斑块的亲和程度有限,甚至不会亲和。ACU193可与广谱的不同可溶性的AβO结合。此外,ACU193 已在离体动物研究中显示出通过抑制AβO的结合来提供对突触毒性的保护原代海马神经元的能力。ACU193还具有合适的体内药理学、靶标参与、血脑屏障渗透和副作用小的特性。在动物模型中进行的非临床研究表明,AβO靶标结合有可能在临床测试的ACU193剂量下实现。最后,在良好实验室规范 (GLP)中,在两种动物物种中进行的毒性研究表明,ACU193具有足够的安全范围。这些数据表明ACU193有可能减少患者认知能力下降。

图片来源:Clinicaltrails
2021年第二季度,Acumen启动了ACU193在早期AD患者中的美国、多中心、随机、双盲、安慰剂对照、单次和多次递增剂量的 1 期临床测试。早期AD患者组由AD导致的轻度痴呆或MCI患者组成,测试排除了中度至重度AD痴呆患者。测试计划在七个队列中招募62名患者,包括单次递增剂量A部分(32名参与者)和重叠的多次递增剂量B部分(30名参与者)。该测试的主要目的是评估静脉输注单次和多次递增剂量的ACU193的安全性、耐受性、药代动力学、药效学和 AβO靶标结合。探索性结果包括认知量表和计算机化认知测试。测试目标是在早期AD患者中建立ACU193机制的证据,以便在2023年快速进入适应性2/3期临床试验。Acumen将定期更新1期试验的状态并预计于2022年底前公布有关安全性和耐受性的临床数据。

图片来源:蹊之美股生物医药
ACU193 1期临床测试计划
4.2 竞争情况
Acumen的竞争对手包括 Alzheon、Alzinova、渤健、Cognition、卫材、礼来等公司。
2021年6月7日,FDA宣布加速审批渤健与卫材联合研发的单抗药物aducanumab上市,用于治疗阿尔兹海默症源性轻度认知障碍(MCI)及轻度阿尔兹海默症。这是自2003年以来,FDA批准的首个阿尔兹海默症治疗新药,也是首个能阻止疾病进展的药物。但FDA这一决定存在很大争议,因为FDA外周和中枢神经系统药物咨询委员会专家大多认为之前的临床试验数据不足以决定性证明aducanumab能有效延缓阿尔兹海默症患者认知功能衰退。但FDA依然批准aducanumab上市。
2021年3月13日,礼来在《新英格兰医学杂志》的一篇文章中表示,其开发的靶向β-淀粉样蛋白(Aβ)的单抗药物Donanemab在2期临床试验中达到主要目标,患者大脑内的β-淀粉样蛋白(Aβ)和Tau淀粉样蛋白沉积得到了有效清除。早期临床试验结果表明,到52周时,接受实验药物的患者的淀粉样斑块水平达到阴性状态。换句话说,他们的淀粉样斑块水平与普通人相同。在275名参与试验的患者中,有一半接受了为期76周的药物治疗,而另一半则接受了安慰剂。涉及的是患有早期症状性阿尔茨海默氏病的人。研究人员还发现该药似乎能使认知能力下降减缓约32%。总体而言,大约40%的接受Donanemab单抗治疗的参与者最早在开始治疗后六个月就达到了淀粉样蛋白阴性,而68%的参与者在18个月内达到了这一目标。尽管结果令人兴奋,但礼来方面表示,为确保Donanemab单抗的安全性,仍需要进行更长且更广泛的试验。
罗氏于2019年已经终止了其药物crenezumab在早期阿尔茨海默病 (AD) 中的III期CREAD1和2临床研究,该决定是基于独立数据监测委员会进行的评估crenezumab安全性和有效性的预先计划的中期分析的结果,该分析表明crenezumab不太可能达到临床痴呆评分总和中从基线变化的主要终点盒数(CDR-SB)分数。在该分析中未观察到crenezumab的安全性信号,总体安全性特征与之前试验中观察到的相似。不过罗氏仍致力于正在进行的阿尔茨海默病临床研究,包括使用其另外两款药物Gantenerumab的GRADUATE III期试验和TAURIEL II期抗tau试验,但这两款药物至今仍未有任何显著成果。
五、融资与合作情况
公司自成立以来融资9000万美元,2018年A1轮1500万,2020年B轮7500万,主要投资者包括BlackRock, PBM Capital, RA Capital, Rock Springs Capital, Sands Capital和其他私募投资者。
IPO前持股>5%的机构如下:

图片来源:公司招股说明书
公司于2021年7月1日上市,发行价为16美元,募集资金1.6亿美元。
六、财务状况
公司目前正处于临床阶段,2019年以及2020年,相应的净亏损分别为791万美元和733万美元,2021年第一季度净亏损为2700万美元。
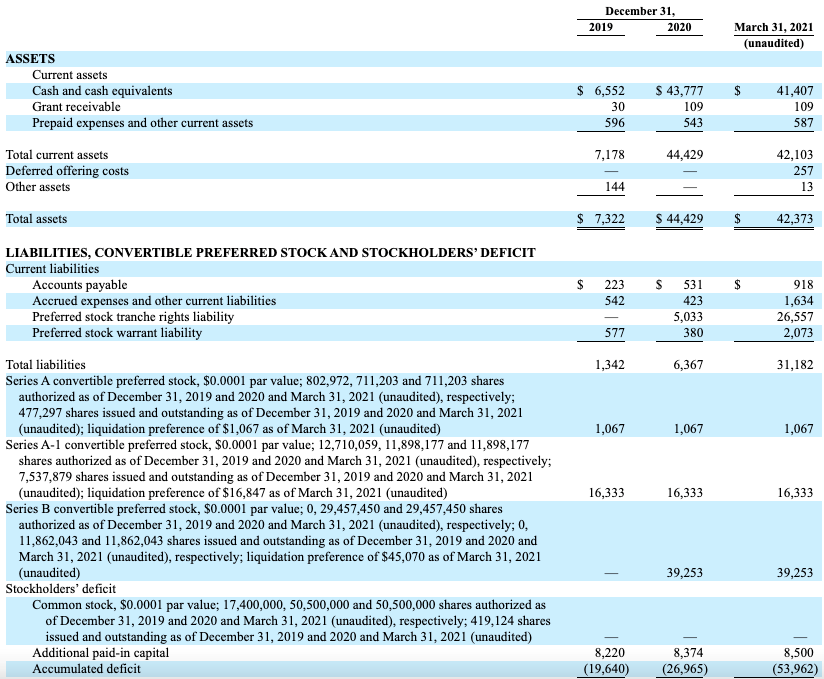

图源:公司招股说明书
公司资产负债表
七、小结
Acumen正在开发一套专有平台用于开发候选产品ACU193,以为目前尚无有效治疗手段的阿尔兹海默症提供一种可行的治疗方式。该公司专注于该领域的研究,目前仅有ACU193一条管线。ACU193 通过阻止AβO与树突棘结合并帮助保护神经元功能来解决阿尔茨海默症的潜在原因。该候选产品相对于其他抗淀粉样蛋白单克隆抗体相比具有特异性高、风险低、疗效好的优势。目前市场上还没有通过审批的有明确疗效的类似药物,唯一获批的渤健的药物aducanumab存在关于疗效的巨大争议。
声明
本报告中部分信息及数据来源于公开可获得资料,对于信息的准确性和完整性不做保证,未经许可,任何机构和个人不得以任何形式翻版、复制及刊登,如需转载请联系授权并需在醒目位置标注转载来源
来源:探针资本